21世紀經濟報道記者季媛媛 上海報道 3月17日22時30分許,藥品專利池組織(Medicines Patent Pool, MPP)正式公開宣布,與包括中國復星醫藥在內的全球35家企業簽訂協議,授權其生產輝瑞口服新冠治療藥物奈瑪特韋(nirmatrelvir)仿制藥,并向覆蓋全球約53%人口的95個中低收入國家供應奈瑪特韋/利托那韋組合包裝產品(Paxlovid),以提高新冠治療藥物在全球中低收入國家或地區的可及性和可負擔性。
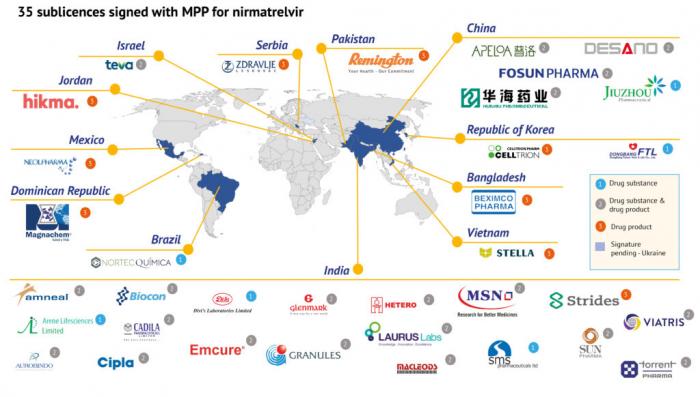
根據MPP官方新聞稿,本次非獨家分許可(The non-exclusive sublicences)允許獲授權的企業生產輝瑞新冠口服藥奈瑪特韋原料藥及其成品藥與利托那韋組合包裝。MPP同時在其新聞稿中表示,本次獲許可的企業證明了他們有能力滿足MPP對生產能力、監管合規以及生產質量符合國際質量標準的藥品的要求。在本次與MPP簽署協議的35家企業中共有5家中國企業,分別是上海迪賽諾、華海藥業、普洛藥業、復星醫藥、九洲藥業。其中,九洲藥業僅獲授權生產原料藥,另外包括復星醫藥在內的4家可同時生產原料藥和制劑。
據了解,本次非獨家分許可并不包括藥物利托那韋(ritonavir)的生產,利托那韋是一種HIV-1蛋白酶抑制劑和CYP3A抑制劑,因其專利權已到期,生產該藥物無需原專利權人許可,獲授權的企業需自行解決藥物利托那韋的供貨。

來源:MPP官網
MPP授權協議落地
藥品專利池(MedicinesPatent Pool, MPP)是2010年在瑞士日內瓦成立的。MPP通過與原研藥企就藥品專利的自愿許可進行談判,原研藥企將其藥品專利放入專利池中,仿制藥企向MPP申請獲得專利池中的專利實施許可,生產并向中低收入國家供應仿制藥。
仿制藥企(主要面向發展中國家制藥企業)一是自愿將其相關藥品專利納入MPP;二是自愿向MPP提交被許可意向,被許可意向經MPP專家評議通過后,MPP與仿制藥公司簽署許可協議,向原研公司給付許可費并向MPP支付中介費。獲得再許可的仿制藥企可被允許在發展中國家生產原研公司的專利藥品,并依照許可協議規定,將所生產的專利藥品銷往低等和中低等收入國家。
MPP許可為非獨占許可,并常通過許可多家仿制藥企業來增加市場競爭,降低藥品價格。概而言之,MPP平衡了原研公司與仿制藥商之間的利益,且有效解決了患者的藥物可及性問題及其與生命健康權之間的沖突問題。現有的MPP許可覆蓋共達131個國家,涵蓋世界銀行標準下所有低收入國家和50%-80%的中等收入國家。
2021年11月,輝瑞宣布,已與聯合國支持的MPP組織達成一項協議,允許其他仿制藥制造商生產其新冠口服藥Paxlovid。該協議使MPP能夠通過向合格的仿制藥制造商授予分許可,促進研究性抗病毒藥物的額外生產和分銷。
根據協議條款,全球獲得授權許可的合格仿制藥企業將能夠向95個國家/地區提供Paxlovid的組合療法,覆蓋全球約53%的人口,包括撒哈拉以南非洲的所有低收入和中低收入國家和一些中高收入國家,以及過去五年中從中低收入狀態轉變為中高收入狀態的國家。
當時,輝瑞公司發言人Kit Longley表示,輝瑞正在“集中努力和資源,以最大限度提高總體供應”。此后不久,輝瑞新冠口服藥Paxlovid陸續在美國、以色列、加拿大、歐洲和日本等地獲批應用。2月12日,國家藥監局公開宣布,根據《藥品管理法》相關規定,按照藥品特別審批程序,進行應急審評審批,附條件批準輝瑞公司新冠病毒治療藥物Paxlovid進口注冊。
至于該藥的售價,輝瑞在美國的定價為:為期5天療程,美國政府需要支付約530美元(約合人民幣3367元)。目前在我國的售價暫未公布。此前輝瑞表示,在疫情期間,會根據每個國家的收入水平進行分層定價,高收入和中高收入國家將比低收入國家支付更多。
哪些原料藥和中間體企業將受益?
此前根據輝瑞財報,2022年計劃生產1.2億個療程Paxlovid(不包含中國市場)。
3月9日,中國醫藥與輝瑞公司簽訂供貨協議,負責Paxlovid在中國大陸的市場的商業運營。隨后3月15日晚,國家衛健委發布《新型冠狀病毒肺炎診療方案(試行第九版)》。在新版診療方案中,加入了兩種抗病毒療法,其中就包括新冠口服藥Paxlovid。不過該藥目前在內地市場尚未正式上市銷售。而據香港特別行政區政府3月15日公報,首批新冠口服抗病毒藥物Paxlovid已于3月14日運抵香港,并于當日送往醫院管理局使用。
“輝瑞已經通過MPP組織授權95個國家生產Paxlovid仿制藥,考慮95個MPP成員國人口已超過全球總人口的一半,市場需求巨大,其最終授權名單落地,上游中間體產業鏈即將迎來巨大需求量和利潤彈性。”民生證券醫藥行業首席分析師周超澤指出,Paxlovid合成路線較復雜,核心中間體SM1和SM2合成具有一定壁壘,考慮時間和設備問題,核心中間體短期供應可能不足,SM1和SM2價格高,毛利率高,尤其是SM1合成涉及-120 ℃超低溫深冷反應資質和氰化物反應,具有較高的生產資質壁壘,也是短期供應存在瓶頸的重要中間體。
據Airfinity數據,該藥生產過程需要從全球供應商大量采購38種不同的原料和試劑。
據中商產業研究院數據,截至2021年11月,我國化學原料藥行業共有35家上市企業,2021年上半年總營收達511.17億元。位列前十名的企業分別為新和成、ST冠福、海正藥業、浙江醫藥、普洛藥業、新華制藥、海普瑞、國邦醫藥,前十家企業2021年上半年總營收達401.74億元,占全部35家上市企業的78.5%。而在新冠口服藥的市場需求推動下,這一市場的空間還會繼續擴大。
以復星醫藥為例,經過在非洲等新興市場超15年的運營,復星醫藥已在非洲39個英語和法語國家及東南亞地區建立了成熟的銷售網絡,這和MPP設定的中低收入國家在地域上有很好地重合。在這些區域,復星醫藥有很好的創新藥和仿制藥商業化經驗,包括注冊、分銷、促銷、藥物安全警戒。此外,復星醫藥向全球公立市場供應了近20年的抗瘧藥產品,積累了豐富的公立市場采購經驗。而這也是繼2022年1月獲MPP授權仿制生產并向105個中低收入國家供應新冠治療口服藥物Molnupiravir后,復星醫藥再獲MPP授權向全球中低收入國家生產及供應新冠治療藥物。
天風證券分析指出,中國作為全球最大的醫藥中間體/原料藥生產和出口地區,在全球醫藥產業鏈占據重要地位,國內原料藥企業具備Nirmatrelvir從原料-中間體-原料藥的全產業鏈供應能力,隨著Paxlovid的多國獲批與MPP協議的全球銷售,Nirmatrelvir合成路線所涉中間體/原料藥的訂單需求有望進一步擴大。
新冠口服藥需求產能有多大?
據輝瑞2月8日公布的2021年業績報告數據顯示,輝瑞在2021年實現營收813億美元,同比大漲92%。其中,口服抗病毒藥物Paxlovid在2021年12月22日獲得FDA的EUA批準后,已拿下美國政府2000萬療程訂單,預計年底將實現1.2億療程產能。根據截至1月底簽署或承諾的供應合同提供的治程劑量,輝瑞Paxlovid 2022年度財務預期收入約220億美元。此外,輝瑞在財報中給出了Paxlovid用于不同突變株的臨床前EC50數據,包括Omicron突變株。
對輝瑞來說,在新冠口服藥上的競爭對手就是默沙東。根據默沙東披露的財報信息,2021年新冠口服藥molnupiravir也貢獻了9.52億美元的收入,預測在2022年molnupiravir的銷售額將達到50億~60億美元,2022年全球銷售額將在561億~576億美元之間。
而在輝瑞之前,藥品專利池組織已在此前1月20日宣布,與包括復星醫藥(600196)、博瑞醫藥(688166)、迪賽諾醫藥、朗華制藥、龍澤制藥在內的全球27家企業簽訂協議,將為全球105個中低收入國家或地區生產及供應高質量、可負擔的默沙東口服抗新冠病毒藥物molnupiravir仿制藥,以促進口服抗新冠病毒藥物在中低收入國家的可負擔性和可及性。另據默沙東公告,截至2021年底已生產1000萬療程Molnupiravir,預計2022年將生產至少2000萬療程Molnupiravir。
天風證券分析指出,從美國政府新冠藥物采購數據可以看出,自新冠口服藥上市后,美國政府采購抗體藥物數量趨勢下降,新冠口服藥物采購趨勢明顯上漲。據各國政府報道,針對輝瑞Paxlovid,美國、英國、日本已分別累計采購2000萬、275萬、200萬療程;針對默沙東molnupiravir,美國、英國、日本已分別累計采購950萬、230萬和160萬療程。
在MPP協議之下,以Paxlovid和molnupiravir為代表的新冠小分子口服藥成為下一個風口。不過,從現有的消息來看,MPP方面表示,制藥商可能準備在今年12月前提供第一批Paxlovid藥片。基于此,分析公司Airfinity估計,更大的數量可能要到2023年5月才能進入市場。
此外,利托那韋口服片是輝瑞新冠口服藥PAXLOVID(300毫克奈瑪特韋片+100毫克利托那韋片組合包裝)的組成之一。據國家藥品監督管理局(NMPA)信息,截至目前,國內共有四家企業獲批生產利托那韋,分別為歌禮藥業、迪賽諾化學、萬全萬特制藥、東陽光藥業。據歌禮制藥-B(01672)公布,已將利托那韋口服片年產能進一步擴大至約5.3億片,以滿足國內和全球日益增長的潛在需求。此外,歌禮已通過歐洲代理商向12個歐洲國家遞交了利托那韋(100毫克薄膜衣片)上市許可申請。此外,精華制藥、海特生物均具有成熟的利托那韋片關鍵中間體生產技術。
如此,在供應規模提升拉動供應鏈需求擴張之下,后續整個中國原料藥市場又會發生怎樣的調整,值得關注。


















 粵公網安備 44010402000579號
粵公網安備 44010402000579號